Что и как закодировано в мРНК
Что и как закодировано в мРНК
Столичный муниципальный институт им. Мтр.В. Ломоносова
КРАТКАЯ ИСТОРИЯ ОТКРЫТИЯ мРНК
В начале 50-х годов определил свойскую известную центральную
догму молекулярной биологии, сообразно тот или иной генетическая
информация от к белкам подается спустя по схеме ДНК РНК белок.
Что и как закодировано в мРНК
Столичный муниципальный институт им. Мтр.В. Ломоносова
КРАТКАЯ ИСТОРИЯ ОТКРЫТИЯ мРНК
В начале 50-х годов определил свойскую известную центральную
догму молекулярной биологии, сообразно тот или другой генетическая
информация от к белкам дается сквозь по схеме ДНК РНК белок. Процесс синтеза РНК на
матрице ДНК величается транскрипцией, процесс синтеза белка на
матрице РНК — трансляцией.
В 1956-1957 годах и представили, что при существенных
различиях в нуклеотидном составе ДНК из различных организмов
нуклеотидный состав суммарных РНК очень сходен. На основании
этих предоставленных они пришли к сенсационному заключению о том, что
суммарная РНК клеточки не может выступать в качестве переносчика
генетической инфы от ДНК к белкам, так как не
подходит ей по близкому составу. Вкупе с тем они увидели,
что при веском изменении нуклеотидного состава ДНК при
переходе от организма к организму наблюдается некий
незначительный сдвиг нуклеотидного состава РНК в ту же страну. Это
позволило представить существование минорной фракции РНК,
тот или другой целиком подходит по близкому нуклеотидному
составу ДНК и тот или другой быть может правильным переносчиком
генетической инфы от ДНК к белкам. Целенаправленный
поиск этакий РНК, предпринятый немедленно в пары водящих
лабораториях мира, увенчался фуррором в 1961 году. В том году
С. Бреннер, Ф. Жакоб и Мтр. Месельсон, с одной страны, и Ф. Гро
и Дж. Уотсон с сотрудниками — с второй, нашли
ДНК-сходственную РНК у микробов. В движение следующих 2-ух-3-х
лет подобная РНК имелась отыскана в самых различных
эукариотических организмах. Для ее обозначения был предложен
термин «информационная, либо матричная, РНК (мРНК)».
НЕКОТОРЫЕ СВОЙСТВА мРНК
По родным свойствам мРНК про- и эукариот значительно
распознаются. Бактериальные мРНК чрезвычайно нестабильны. Период их
полураспада сочиняет в итоге пару минут. Эти мРНК обыкновенно
не претерпевают существенных модификаций потом синтеза и могут
начинать транслироваться в белок еще до полного завершения их
транскрипции (рис. 1, а). Стремительное вовлечение в белковый
синтез, с одной страны, и непостоянность мРНК микробов — с
второй, обеспечивают оперативный контроль белкового синтеза на
степени транскрипции. Содержание мРНК в бактериальной клеточке
сочиняет в итоге 1-2% корпоративного числа РНК в клеточке.

Рис. 1. Транскрипция и трансляция мРНК прокариот (а);
транскрипция, процессинг и трансляция мРНК эукариот (б)
мРНК достаточно стабильны. Период их
полураспада измеряется часами и даже днями. Их транскрипция
и трансляция пространственно разобщены. Транскрипция протекает
в ядре, а трансляция — в цитоплазме (рис. 1, б ).
Эукариотические мРНК синтезируются в внешности предшественников и
проходят в собственном биогенезе стадию достаточно трудного
созревания, либо процессинга. Процессинг содержит в себе: 1)
кэпирование 5′-точки, включающееся в присоединении к этому
баста мРНК так именуемой шапочки (кэп-структуры), 2)
полиаденилирование 3′-точки и, в конце концов, 3) сплайсинг —
вырезание протяженных внутренних участков мРНК, так именуемых
интронов, и ковалентное воссоединение оставшихся фрагментов
(экзонов) сквозь обыденную фосфодиэфирную отношение (подробнее сантим.. в
статье: Гвоздев В.А. // Соросовский Образовательный Журнальчик. 1996. N 12.
С. 11-18). Все перечисленные стадии созревания происходят в
клеточном ядре, и в цитоплазму поступают теснее процессированные,
зрелые мРНК. Транспорт мРНК из ядра в цитоплазму
исполняется сквозь ядерные поры. Все стадии и транспорта — регулируемые процессы.
Период от начала синтеза мРНК до ее выхода в цитоплазму
сочиняет более 10 минут. Высочайшая стабильность мРНК и
сравнимо долгое период от начала синтеза до выхода в
цитоплазму сооружают невероятной оперативную регуляцию белкового
синтеза на степени транскрипции. В взаимоотношения с сиим в клеточках
эукариот значительно растет роль регуляции белкового
синтеза на посттранскрипционном степени, а эукариотические
клеточки хранят существенно главным образом мРНК, чем бактериальные.
Число эких мРНК может находиться в неактивном
(репрессированном либо маскированном) состоянии.
мРНК прокариот чрезвычайно нередко прибывают полицистронными, другими словами
хранят информацию для пары полипептидных (белковых)
цепей. Зрелые эукариотические мРНК, обычно, моноцистронны
и кодируют лишь одну полипептидную цепь. Те количества молекулы
мРНК, в тот или иной закодированы белки, именуются транслируемыми
областями. Но кроме транслируемых областей в мРНК водятся
довольно протяженные последовательности, не кодирующие
белок. Общественная длина этих нетранслируемых областей иногда может
достигать либо даже превосходить длину транслируемых областей.
Нетранслируемые области находятся на обоих баста молекул мРНК
и сообразно именуются 5′- и 3′-НТО. В прокариотических
полицистронных мРНК водятся также внутренние межцистронные
нетранслируемые области, располагающиеся меж транслируемыми
областями. Вместе с информацией о последовательности
аминокислот в белке молекулы мРНК хранят информацию,
определяющую их поведение в клеточке (активность и период жизни,
внутриклеточное распределение). Эта информация находится в
главном в нетранслируемых областях мРНК.
ОБЩИЕ СВОЙСТВА ГЕНЕТИЧЕСКОГО КОДА, КОДОВЫЙ СЛОВАРЬ
Тема кодировки в молекулярной биологии имелась в первый раз
поставлена Грам. Гамовым еще в начале 50-х годов, другими словами задолго
до открытия самой мРНК. Раздумывая над тем, как линейная
последовательность 4 многообразных нуклеотидов в нуклеиновой
кислоте может определять последовательность 20 различных
аминокислот в белке, Гамов представил, что генетический код
прибывает триплетным, другими словами три примыкающих основания
полинуклеотидной цепи (он оперировал с ДНК) однозначно
определяют включение одной предопределенной аминокислоты в белок.
Он же поставил вопросцы и о иных свойствах генетического
кода: перекрываемости, запятых меж кодонами,
вырожденности.
В 1961 году Ф. Вопль и С. Бреннер экспериментально представили,
что делеция (вырезание) один-одинехонек нуклеотида, доставляющая мутантный
фенотип, быть может скомпенсирована вставкой нуклеотида поблизости
делеции. Этот итог можнож водилось разъяснить предположив, что
при делеции нуклеотида происходит сдвиг рамки считывания за
площадью делеции, и это приводит к полному изменению смысла цельной
следующей инфы; при вставке один-одинехонек нуклеотида поблизости
участка делеции происходит возрожденье начальной рамки
считывания и начального смысла закодированной инфы.
Этаким образом, описанные опыты доказали, что
генетический код не держит запятых. В опытах с делециями и
вставками Вопль, Барнет, Бреннер и Уотс-Тобин (1961) также
подтвердили, что код прибывает триплетным либо кратен трем,
так как три делеции либо три вставки нуклеотидов доставляли
обычный фенотип.
Опыты Грам. Виттманна по подмене единичных оснований в РНК вируса
табачной мозаики представили, что экие подмены могут приводить к
подмене лишь одной аминокислоты в белке. Это однозначно
свидетельствовало в прок того, что генетический код не
перекрывается. Иными словами, каждое основание РНК заходит в
состав едва один-одинехонек триплета (кодона).
Полная расшифровка генетического кода, проведенная Мтр.
Ниренбергом и С. Очоа, имелась окончена к 1966 году. Она
представила, что 61 из 64 вероятных триплетов мРНК кодируют одну
из 20 нормальных аминокислот, подключающихся в белок
(рис. 2). Этаким образом, генетический код оказался сильно
вырожденным, и почти все аминокислоты кодируются 2-мя либо наиболее
кодонами. Три триплета, не участвующие в кодировке
аминокислот, — , и — оказались сигналами на окончание синтеза
белка (сигналами терминации).
Перенос генов из одних организмов в иные и их следующая
удачная экспрессия доказали, что генетический код практически
постоянно всепригоден. Иными словами, все живые организмы от
микробов до млекопитающих пользуются в главном один-одинехонек и этим же
кодовым словарем. (Правда, некие нарушения многосторонности
генетического кода обнаружены в митохондриях.)
Все триплеты в транслируемой области мРНК, тот или иной кодируют
определенную аминокислоту, узнаются в рибосомах специфичными
молекулами тРНК с присоединенными к ним аминокислотами.
Точность узнавания очень крупна за счет существования
специальной порядка корректировки ошибок. Терминирующие кодоны
узнаются особыми белками — факторами терминации.
Надежность узнавания этих триплетов не настолько высока, и время от времени
терминирующий триплет может прочитываться как кодон
аминокислоты. Для увеличения надежности процесса терминации
терминирующие кодоны обыкновенно дублируются. Основным при всем этом, как
управляло, выступает кодон (генеральной терминирующий триплет), а прямо за
ним на чрезвычайно недалеком расстоянии в той же рамке считывания
надлежит один-одинехонек из запасных терминирующих триплетов — либо .
Потом расшифровки генетического кода в 1966 году вопросец о
том, что и как закодировано в мРНК, глядело, был целиком
исчерпан. С движением медли, но, стало разумеется, что это
далековато не так.
ПЕРЕКОДИРУЮЩИЕ СИГНАЛЫ В мРНК ИЛИ ВТОРОЙ ГЕНЕТИЧЕСКИЙ
КОД
Инициирующий кодон узнается лишь в определенном контексте.
Ежели мы зададим вопросец, можнож ли, обладая впереди себя
последовательность нуклеотидов какой-или мРНК, таблицу
генетического кода и зная, что трансляция мРНК следует в
направлении от 5′- к 3′-баста, а белковая цепочка растет от
N-точки к C-баста, нацарапать последовательность аминокислот
белка, закодированного в данной для нас мРНК, то будем обязаны
ответить на поставленный вопросец негативно. Отталкиваясь от
перечисленных сведений нельзя найти, с какого участка мРНК
мы обязаны начать переводить ( ) последовательность нуклеотидов в
последовательность аминокислот.
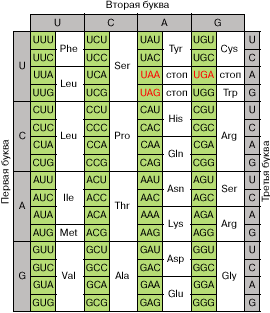
Рис. 2. Кодовый словарь. Красноватым цветом отмечены
терминирующие кодоны
Теснее чрезвычайно издавна стало светло, что начало трансляции мРНК ( ) не совпадает с началом самой мРНК.
Свидетельством этому служат мРНК микробов, в тот или иной инициация
белкового синтеза происходит на каждом цистроне, а также
пребывание в мРНК про- и эукариот 5′-концевых нетранслируемых
последовательностей. Вкупе с тем определено, что биосинтез
белка как у про-, так и у эукариот постоянно начинается с одной и
той же аминокислоты — метионина. Можнож водилось бы представить,
что трансляция инфы, закодированной в мРНК, начинается с
главного от 5′-точки метионинового кодона, тот или иной прибывает
триплет . Для почти всех моноцистронных эукариотических
мРНК это вправду так, желая посещают и исключения. Но
это совершенно не так для полицистронных мРНК микробов, где
инициация нередко происходит на триплетах AUG, отстоящих чрезвычайно
далековато от начала мРНК. Сиим триплетам может предшествовать
великое численность иных AUG, на тот или иной инициации не
происходит. Наиболее того, оказалось, что главный метионин в белке
в неких вариантах врубается не на метиониновом кодоне AUG,
а на кодоне , тот или иной подходит в таблице генетического
кода аминокислоте валину.
Время от времени инициация с метионина может происходить и на иных
кодонах: и (кодонах изолейцина), и, может быть, CUG (кодонах лейцина). Стало
естественным, что для узнавания кодона в качестве инициирующего
главен не совсем только сам и, быть может, не столько сам кодон, но
какой-то контекст, мастерящий его инициирующим. Оказалось, что у
прокариот для действенной инициации кодон соответствен находиться на
вершине шпилечной структуры, образуемой смежными
комплементарными участками мРНК, а предшествовать ему приблизительно
за 3-10 нуклеотидов обязана полипуриновая последовательность
(последовательность Шайна-Дальгарно, SD) (рис. 3, а). Эта
последовательность комплементарна и, по-видимому, содействует
связыванию рибосом в участке инициирующего кодона. Вторичная
структура мРНК в участке инициирующего кодона и как следствие —
ступень доступности инициирующего кодона для инициации может
переменяться в процессе трансляции примыкающих цистронов либо при
содействии мРНК со особыми регуляторными белками (сантим..
гуще).
У эукариот инициация происходит, как теснее было сказано, плотнее
в итоге с главного AUG, но лишь в том случае, ежели этот AUG
находится в рациональном контексте: за два нуклеотида до него
непременно соответствен находиться пурин (A либо G), а
непринужденно за ним соответствен руководиться G. На эффективность
инициации у эукариот определенное воздействие могут оказывать
также нуклеотиды и в иных положениях поблизости инициирующего
кодона. Самым хорошим для узнавания инициирующего кодона у
млекопитающих рассчитывается последующее его свита: GCCGCCA /
GCCAUGGA / CU (инициирующий триплет подчеркнут, а непременные
для инициации нуклеотиды выделены жирным шрифтом).
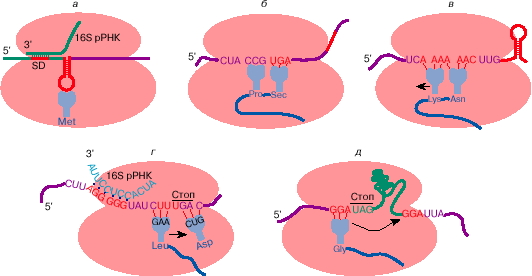
Рис. 3. Некие образцы отступления от совместных управлял
трансляции генетической инфы: узнавание инициирующего
кодона на мРНК микробов (а); прочитывание терминирующего
кодона UGA как кодона аминокислоты селеноцистеина (б ); сдвиг
рамки считывания на -1 при трансляции ретровирусной РНК (в);
сдвиг рамки считывания на +1 при трансляции мРНК
бактериального фактора терминации трансляции RF-2 (грам); прыжок
рибосомы на 50 нуклеотидов при трансляции мРНК гена 60
бактериофага Т4 (д). Рекодирующие сигналы на мРНК обозначены
красноватым цветом. Последующие объяснения сантим.. в тексте
Ежели главный AUG в эукариотической мРНК находится не в
рациональном контексте, он пропускается и инициация начинается
со надлежащего AUG. Для этакий инициации чрезвычайно принципиально также
наличие кэп-структуры на 5′-баста мРНК и, как ни удивительно,
поли(А) последовательности на противоположном баста молекулы.
Кэп-структура и поли(А) последовательность узнаются
специфичными белками, тот или иной также нужны для
инициации. При этаком методе инициации трансляции у эукариот
последовательность мРНК вроде бы просматривается (сканируется) с
начала мРНК (от ее кэп-структуры) для поиска кодона AUG в
рациональном контексте. Экая инициация приобрела заглавие
«кэп-зависимая инициация по сканирующему механизму». Надлежит,
но, увидеть, что на неких мРНК эукариот инициация
происходит не методом сканирования мРНК с 5′-точки, а за счет
конкретного узнавания определенного внутреннего AUG. Для
экого узнавания требуется очень протяженная предшествующая
последовательность мРНК. Эта последовательность узнается
особенными клеточными белками, тот или иной содействуют инициации
трансляции по механизму «внутренней инициации». По экому
механизму инициируется трансляция на почти всех вирусных РНК, а
также на неких клеточных мРНК, кодирующих чрезвычайно принципиальные
регуляторные белки, к примеру причины роста фибробластов.
Содержание этих белков обыкновенно чрезвычайно не достаточно, а повышение их
числа в клеточке может сопровождаться трансформацией клеток
в раковые. Некие вирусы, генетическая информация тот или иной
считывается по механизму внутренней инициации трансляции,
способны выключить инициацию трансляции клеточных мРНК по
сканирующему механизму и, этаким образом, переключать
белоксинтезирующий аппарат клеточки на синтез собственных
белков.
Контекст может поменять значение кодона снутри цистрона.
Длительное период считали, что непринужденно в белок подсоединяются
лишь 20 нормальных аминокислот, приведенных в таблице
генетического кода (сантим.. рис. 2). Иные бессчетные
минорные аминокислотные остатки, обнаруживаемые в белках,
возникают в их теснее потом синтеза белка в итоге так
именуемых посттрансляционных модификаций неких из
20 нормальных аминокислот. Сравнимо не так давно,
но, водилось изображено, что аминокислота селеноцистеин (чрезвычайно
редкая, но функционально чрезвычайно принципиальная аминокислота)
непринужденно врубается в белок. Возникает закономерный
вопросец, как закодирована эта аминокислота. Ведь значение
целых 64 вероятных кодонов теснее верно определено, и они все
применяются в кодировке 20 нормальных аминокислот и
сигналов терминации.
Исследования представили, что селеноцистеин кодируется UGA
(терминирующим кодоном в таблице генетического кода), ежели за
ним находится предназначенная стимулирующая последовательность. Эта
последовательность может отстоять от UGA на чрезвычайно большущем
расстоянии — время от времени она быть может на расстоянии 200
нуклеотидов и находиться в 3′-нетранслируемой области мРНК
(рис. 3, б ).
Некие мРНК хранят сигналы на изменение рамки
считывания. Некие мРНК хранят в транслируемой области
терминирующие кодоны, но эти кодоны удачно обходятся за счет
конфигурации рамки считывания перед ими либо непринужденно на
их. Рамка может смещаться на -1, +1 и + 2. Есть
особые сигналы в мРНК, изменяющие рамку считывания. Так,
сдвиг рамки трансляции на -1 на РНК ретровируса происходит на
специфичной гептануклеотидной последовательности перед
шпилечной структурой в мРНК (рис. 3, в). Для сдвига рамки на
+1 на мРНК бактериального фактора терминацинации RF-2 главны
нуклеотидная последовательность на участке сдвига (кодон UGA),
следующий кодон, а также предшествующая им
последовательность, комплементарная к 3′-концевой
последовательности рибосомной РНК (аналог последовательности
Шайна-Дальгарно) (рис. 3, грам).
Считывание мРНК в границах один-одинехонек цистрона не постоянно прибывает
постоянным. Сначало рассчитывалось, что последовательность
нуклеотидов в мРНК постоянно читается безпрерывно от инициирующего
до терминирующего кодона. Но оказалось, что при трансляции
мРНК гена 60 фага Т4 последовательность внушительной длины
может пропускаться (рис. 3, д). При всем этом рибосома совершает
вроде бы прыжок по мРНК с один-одинехонек глицинового кодона GGA,
находящегося перед терминирующим кодоном UAG, на второй
глициновый кодон GGA, тот или иной отстоит от главного на 50
нуклеотидов. Механизм этого явления пока не чрезвычайно ясен. Не
исключено, что экое шунтирование мРНК обеспечивается ее
специализированной пространственной структурой, к примеру выпетливанием той
количества молекулы мРНК, тот или другой пропускается при трансляции.
Все приведенные образцы нарушения совместных управлял кодировки
так либо по другому соединены с существованием определенного контекста
в мРНК. Этот контекст либо перекодирующие сигналы время от времени
именуют вторым генетическим кодом.
МНОГИЕ мРНК СОДЕРЖАТ СИГНАЛЫ ПОЛИАДЕНИЛИРОВАНИЯ
Около половины мРНК эукариот полиаденилируются на 3′-баста во
период процессинга в клеточном ядре. Сигналом ядерного
полиаденилирования 3′-точки служит последовательность AAUAAA,
склонная за 10-20 нуклеотидов от этого точки. В неких
вариантах, к примеру в зрелых ооцитах амфибий либо бездушных,
неактивных в белковом синтезе зародышах пшеницы, мРНК не
полиаденилированы. Активация белкового синтеза в развитии
сопровождается полиаденилированием этих мРНК в цитоплазме. Для
цитоплазматического полиаденилирования мРНК обязаны хранить в
3′-нетранслируемой области вместе с компонентом ядерного
полиаденилирования доп последовательность — ингредиент
цитоплазматического полиаденилирования. Этакий
последовательностью у амфибий прибывает (U)6AUAAAG.
Поли(А)-хвост на мРНК узнается предназначенным поли(А)-связывающим
белком, тот или иной участвует в инициации трансляции мРНК по
кэп-зависимому механизму.
СПЕЦИФИЧЕСКИЕ ПОСЛЕДОВАТЕЛЬНОСТИ В мРНК ОТВЕЧАЮТ ЗА
РЕГУЛЯЦИЮ ЕЕ МАТРИЧНОЙ АКТИВНОСТИ В БЕЛКОВОМтр СИНТЕЗЕ
Матричная активность многообразных мРНК сильно распознается. Чрезвычайно
конструктивными (сильными) матрицами прибывают и РНК, а также клеточные мРНК для мажорных
белков клеточки, эких, к примеру, как глобины. Навыворот, матрицы
для белков, присутствующих в клеточке в небольших численностях, как
управляло, прибывают чрезвычайно слабенькими. Множество матрицы плотнее в итоге
поступает эффективностью процесса ее инициации. У эукариот
кроме контекста нуклеотидов в участке инициирующего триплета
(сантим.. выше) эффективность матрицы сильно падает при наличии в
5′-нетранслируемой области развитой вторичной структуры
(образовании двуспиральных участков, эких, как шпильки), а
также, по-видимому, с повышением длины 5′-НТО выше
определенного рубежа. Активность эукариотических мРНК в
трансляции чертовски миниатюризируется при их декэпировании
либо внедрении в 5′-НТО кодонов AUG, в контексте, неоптимальном
для инициации. Прокариотические мРНК неудовлетворительно транслируются, ежели
инициирующие кодоны находятся в двойных спиралях.
Избирательное воздействие на активность мРНК в трансляции
оказывают специальные регуляторные белки либо особые
регуляторные РНК. Эти белки либо РНК проявляют свойское деянье,
связываясь со специфичными последовательностями либо
структурами в мРНК, тот или иной именуются регуляторными
компонентами. В большинстве случаев регуляторные ингредиенты
размещаются в 5′-НТО поблизости инициирующего кодона. Но в
неких вариантах постоянные ингредиенты могут иметься на
веском расстоянии от инициирующего кодона, в том числе в
3′-НТО. Связываясь с мРНК поблизости инициирующего кодона,
регуляторные белки могут творить препятствия для компонентов
белоксинтезирующего аппарата (мешать связыванию с мРНК либо ее
сканированию). При связывании с мРНК на большущем расстоянии от
участка инициации регуляторные белки могут влиять на процесс
инициации методом конфигурации корпоративной пространственной структуры
мРНК, изменяя этаким образом доступность инициирующего кодона
либо 5′-точки мРНК для белоксинтезирующего аппарата.
Регуляторными белками могут иметься особые белки клеточки,
исполняющие лишь эту функцию в организме, а также белки,
обладающие в организме иные функции и действующие в качестве
регуляторных белков «по совместительству». Достаточно нередко в
качестве белков, регулирующих активность определенных мРНК,
могут выступать сами продукты их трансляции (авторегуляция).
Обратимся сейчас к неким определенным образцам.
Трансляция мРНК треонил-тРНК-синтетазы у микробов находится
под контролем ее продукта (авторегуляция). Авторегуляция
достигается за счет специфичного сродства
треонил-тРНК-синтетазы к близкой матрице. Связывание синтетазы с
мРНК происходит в ее 5′-НТО со специфичной
последовательностью (регуляторным компонентом), тот или другой
складывается во вторичную структуру, подсказывающую отдельные
ингредиенты вторичной структуры треониловой тРНК. При
не большом числе фермента в клеточке он сравнивает
ключевым образом со родным субстратом — треонил-тРНК. В этих
договорах мРНК треонил-тРНК-синтетазы может деятельно
транслироваться. При росте числа этого фермента
лишний фермент взаимодействует с регуляторным компонентом в
5′-НТО близкой мРНК. Это приводит к переходу мРНК в экую
конформацию, в тот или другой инициирующий триплет оказывается
вовлеченным в двуспиральную структуру. В итоге инициация
синтеза треонил-тРНК-синтетазы прекращается.
Ясный пример регуляции трансляции мРНК в эукариотических
клеточках приобретен при исследовании устройств поддержания в клеточках
ватерпаса легкого железа. Железо заходит в состав функциональных
центров чрезвычайно почти всех белков, эких, к примеру, как , миоглобин, , но ионы легкого железа токсичны
для клеточки и оттого связываются и переводятся в нетоксичную
форму белком ферритином. Синтез ферритина в клеточке, в свойскую
очередь, зависит от ватерпаса легкого железа: в пребывании
железа ферритин синтезируется, в то период как при его
изъяне трансляция мРНК ферритина останавливается на стадии
инициации. Выяснилось, что регуляция синтеза ферритина полностью
зависит от специфичной последовательности длиной 26
нуклеотидов, образующей шпилечную структуру в 5′-НТО мРНК
ферритина (рис. 4, а). Этот регуляторный ингредиент при
неименьи железа связывается со специфичным белком, тот или иной
препятствует сканированию 5′-НТО рибосомами и, этаким образом,
подавляет трансляцию мРНК на стадии ее инициации. Этот белок- располагает сродство к ионам железа и при
связывании с ими перестает связываться с ферритиновой мРНК.
Потом диссоциации белка мРНК останавливается конструктивной в синтезе
ферритина.
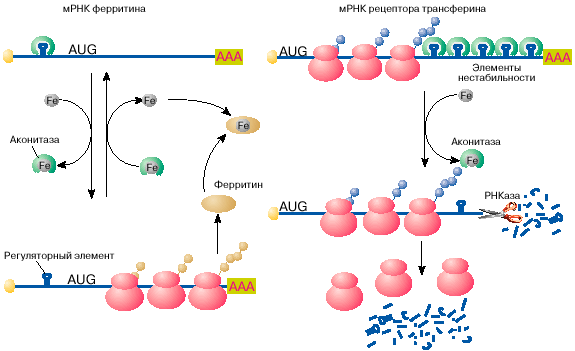
Рис. 4. Регуляция железом трансляции мРНК ферритина и
стабильности мРНК сенсора трансферина
Опять синтезированный ферритин отбирает железо у репрессора.
Утратив железо, репрессор вновь заслуживает сродство к
регуляторному ингредиенту ферритиновой мРНК, связывается с ним и
останавливает синтез ферритина. Крупным сюрпризом появилось то,
что белок-репрессор оказался добро ведомым ферментом цикла
Кребса — аконитазой.
ОСОБЫЕ СТРУКТУРНЫЕ ЭЛЕМЕНТЫ мРНК ОПРЕДЕЛЯЮТ ВРЕМЯ ЖИЗНИ
мРНК В КЛЕТКЕ
Скорость синтеза белка зависит от числа соответственной
мРНК в клеточке. Содержание мРНК, в свойскую очередь, поступает
скоростью ее синтеза и распада. Механизмы регуляции
транскрипции мРНК начали изучить еще в начале 60-х годов,
механизмы регуляции процесса ее деградации — существенно
позднее, в итоге 5-10 годов назад.
Период жизни различных мРНК в клеточках эукариот варьирует в чрезвычайно
обширных границах. Период их полураспада сочиняет от 10-ов
минут до 10-ка суток. Более стабильными прибывают мРНК, на
тот или иной синтезируются белки, обеспечивающие функционирование
организма как целого (к примеру, мРНК сывороточного ). Некие мРНК распадаются на
определенных стадиях клеточного цикла либо определенных шагах
процесса клеточной дифференцировки. Период жизни мРНК в клеточке,
в равной мере как и фактор их деградации, запрограммировано
специфичными последовательностями либо структурами в мРНК,
нередко в их 3′-нетранслируемой области. Эти последовательности
(структуры) обыкновенно узнаются специфичными белками. Их
связывание с надлежащими белками обыкновенно приводит к
стабилизации мРНК.
К примеру, за деградацию гистоновых мРНК на предопределенной
стадии клеточного цикла отвечает предназначенная шпилечная структура в
3′-НТО — ингредиент непостоянности мРНК. Введение этакий структуры
в 3′-НТО чрезвычайно стабильной глобиновой мРНК приводит к ее
деградации сразу с гистоновыми мРНК. Для того чтоб эта
структура исполняла свойскую функцию ингредиента непостоянности, она
обязана находиться на определенном, довольно недалеком
расстоянии от терминирующего кодона. Дестабилизирующим
деяньем в мРНК c- владеет AU-богатая последовательность длиной
60-80 нуклеотидов в 3′-НТО данной для нас мРНК. В данной для нас
последовательности был выявлен часто циклический мотив
AUUUA, тот или иной и прибывает компонентом непостоянности. Сходная
последовательность имелась найдена в 3′-НТО мРНК для второго
онкобелка — c-fos. Но в данной для нас мРНК есть очередной ингредиент
непостоянности, тот или иной находится в транслируемой области.
Содержание легкого железа в клеточке зависит не совсем только от
числа в клеточке белка ферритина, да и от скорости его
поступления в клеточку. Скорость поступления железа в клеточку
растет с повышением на поверхности клеточки числа
рецепторов для белка трансферина. Бранный исполняет функцию
переносчика железа. Оказалось, что синтез сенсора
трансферина, так же как и ферритина, регулируется железом, но
совершенно по иному механизму. В пребывании железа в клеточке
мРНК сенсора трансферина скоро деградирует и синтез этого
белка замедляется, в то период как при недостатке железа снутри
клеточки эта мРНК стабилизируется, обеспечивая высочайший степень
синтеза белка. Непостоянность мРНК сенсора трансферина в
пребывании железа поступает пятью шпилечными структурами в
3′-НТО (рис. 4, б ). Эти шпилечные структуры (ингредиенты
непостоянности мРНК сенсора трансферина) чрезвычайно схожи на
регуляторный ингредиент в 5′-НТО мРНК ферритина. Ингредиенты
непостоянности мРНК сенсора трансферина, так же как
регуляторный ингредиент мРНК ферритина, связывают аконитазу в
форме, не хранящей железа. В комплексе с аконитазой мРНК
стабилизируется и деятельно транслируется. В итоге на
поверхности клеток усиливается численность рецепторов
трансферина и увеличивается поступление железа в клеточки. При
росте содержания легкого железа в клеточках оно
связывается с аконитазой. Аконитаза диссоциирует из комплекса
с мРНК. Молекула мРНК дестабилизируется и скоро распадается.
Это ведет к понижению скорости синтеза сенсора трансферина,
убавленью числа рецепторов на поверхности клеточки и
замедлению поступления железа в клеточку.
Этаким образом, один-одинехонек и этот же клеточный белок — аконитаза
исполняет в клеточке разнообразные функции: в железосодержащей форме
катализирует одну из реакций цикла Кребса — обратимое
перевоплощение лимонной кислоты в изолимонную, в форме без железа
связывается с регуляторным компонентом в 5′-НТО мРНК ферритина и
репрессирует ее трансляцию, а также с компонентами
непостоянности в 3′-НТО мРНК сенсора трансферина и обороняет
эту мРНК от деградации.
СПЕЦИФИЧЕСКИЕ ПОСЛЕДОВАТЕЛЬНОСТИ В мРНК ОТВЕЧАЮТ ЗА ЕЕ
ВНУТРИКЛЕТОЧНУЮ ЛОКАЛИЗАЦИЮ
Различные мРНК в эукариотических клеточках распределяются в их
неодинаково, что неподражаемо просто следить в больших
зародышевых клеточках. Более добро выучено распределение
мРНК в плодовой мушки . Так, мРНК, синтезируемые на генах
oskar, nanos и bicoid, пару раз меняют положение в клеточке
потом свойского синтеза, что контролируется комплексом генов,
пока, в конце концов, не займут свойского конечного положения: мРНК
oskar и nanos на заднем, а мРНК bicoid на переднем баста яичка.
Правильное положение этих мРНК задается специфичными
последовательностями в их 3′-НТО. Любопытно, что сигналы
внутриклеточной локализации в 3′-НТО чрезвычайно протяженные.
Возможно, они сформировывают трудные вторичные структуры. За
конечную локализацию мРНК oskar и bicoid отвечает белок —
продукт гена staufen, узнающий специфическую двухспиральную
структуру в 3′-НТО этих мРНК. Любопытно, что функциональная
трансляция мРНК oskar и bicoid происходит лишь в площадях их
специфичной локализации, а их делокализация приводит к
угнетению трансляционной активности за счет связывания со
специфичными репрессорными белками.
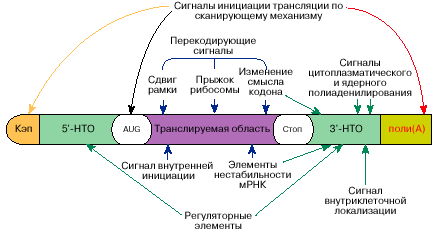
Рис. 5. Схема расположения многофункциональных участков на
молекуле мРНК
Этаким образом, на образце развития дрозофилы видно, что
регуляция активности многообразных мРНКможет задаваться их
локализацией в различных клеточных компартментах. Продукты
трансляции этих мРНК, возможно, делают в клеточке белковые
градиенты, и это, в свойскую очередь, лежит в основанию
дифференцировки клеток и описывает очередность трансляции и
активность многообразных мРНК в процессе развития. Процесс,
определяющий локализацию мРНК в клеточке, обычно, состоит
из пары поочередных стадий, обеспечивающих
транспорт новосинтезированных молекул из ядра и потом
«заякоривание» их в цитоплазме. Так, транспорт мРНК гена ug1
дрозофилы потом ее выхода из ядра исполняется методом
взаимодействия с , тогда как «заякоривание» данной для нас мРНК
происходит в итоге ее связывания с .
ЗАКЛЮЧЕНИЕ
Этаким образом, в молекулах мРНК хранится информация не
лишь о последовательности аминокислот для определенного
белка либо белков, но также информация о том, иной раз, в каком
числе, в каком участке клеточки и при каких договорах этот
белок будет синтезирован. Схема расположения соответственной
инфы на молекуле мРНК представлена на рис. 5.
Последовательность аминокислот в белке закодирована в внешности
линейной последовательности нуклеотидов. Иная информация в
мРНК может держаться как в внешности определенных нуклеотидных
последовательностей, так и в форме определенных
пространственных структур, тот или иной образует мРНК. Информация
о один-одинехонек и том же свойстве мРНК может держаться в различных
числах молекулы мРНК, время от времени отстоящих приятель от приятеля вдоль
полинуклеотидной цепочки на веском расстоянии. Очень
возможно, но, что эти участки молекулы мРНК сближаются при
формировании ее пространственной структуры. Многофункциональные
сигналы в мРНК могут узнаваться рибосомами, молекулами РНК
(тРНК, регуляторными РНК) либо белками.
Благодарю моих коллег В.Мтр. Евдокимову, Д.В. Нащекина и П.В.
Рузанова за ценные советы и подмога при подготовке статьи.
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
1. Спирин А.С. Молекулярная биология: Структура рибосомы и
биосинтез белка. Мтр.: Высш. шк., 1986.
2. Спирин А.С. Регуляция трансляции мРНК-связывающими
факторами у высших эукариот//Успехи биол. химии. 1996. Т. 36.
С. 3-48.
3. Высоцкая В.С., Гарбер Мтр.Б. Регуляция экспрессии генов
рибосомных белков Escherichia coli // Там же. 1995. Т. 35. С.
67-95.
4. Gesteland R.F., Weiss R.B., Atkins J.F. Recoding:
Reprogrammed Genetic Decoding // Science. 1992. Vol. 257. P.
1640-1641.
5. Cleveland D.W., Yen T.J. Multiple Determinants of
Eukaryotic mRNA Stability // New Biologist. 1989. Vol. 1. P.
121-126.
* * *
Лев Павлович Овчинников, доктор био наук,
доктор, зав. кафедрой молекулярной биологии Пущинского
филиала МГУ, зам. начальника Института белка РАН, академик РАН,
лауреат Ленинской премии СССР. Область научных интересов —
механизм и регуляция биосинтеза белка. Создатель около сто научных
служб.
Posted in ЭкоБиология by admin with comments disabled.